圣路易斯华盛顿大学的研究团队发现,需要识别MHCII类抗原才激活的CD4+T细胞,也就是辅助性T细胞的免疫应答,对CD8+效应T细胞的抗癌起着重要作用,两种T细胞必须协同作战,才能激活足够强大的抗癌免疫杀伤[1]!
很长时间以来,科学家们对免疫治疗和治疗中免疫细胞的关注,都集中在了身处最前线的效应T细胞身上,毕竟它们是识别和杀伤癌细胞的主力嘛,而辅助T细胞的作用却不够明确,有人认为它们可有可无,甚至会“拖后腿”。
这一方面是因为效应T细胞可以直接杀伤癌细胞,另一方面则是因为癌细胞新抗原的特殊性。大多数能够激活抗肿瘤免疫的癌细胞新抗原,从种类上来说属于主要组织相容性复合体(MHC)I类限定分子[2],它们只能被效应T细胞识别。
而能被辅助性T细胞识别的MHCII类限定分子,在已知的新抗原中寥寥无几,因此对辅助性T细胞的研究,也往往只是从过往已知的对效应T细胞的分化和增殖入手。它亲自下场识别MHCII类新抗原,并不被认为是免疫治疗起效的必要条件。
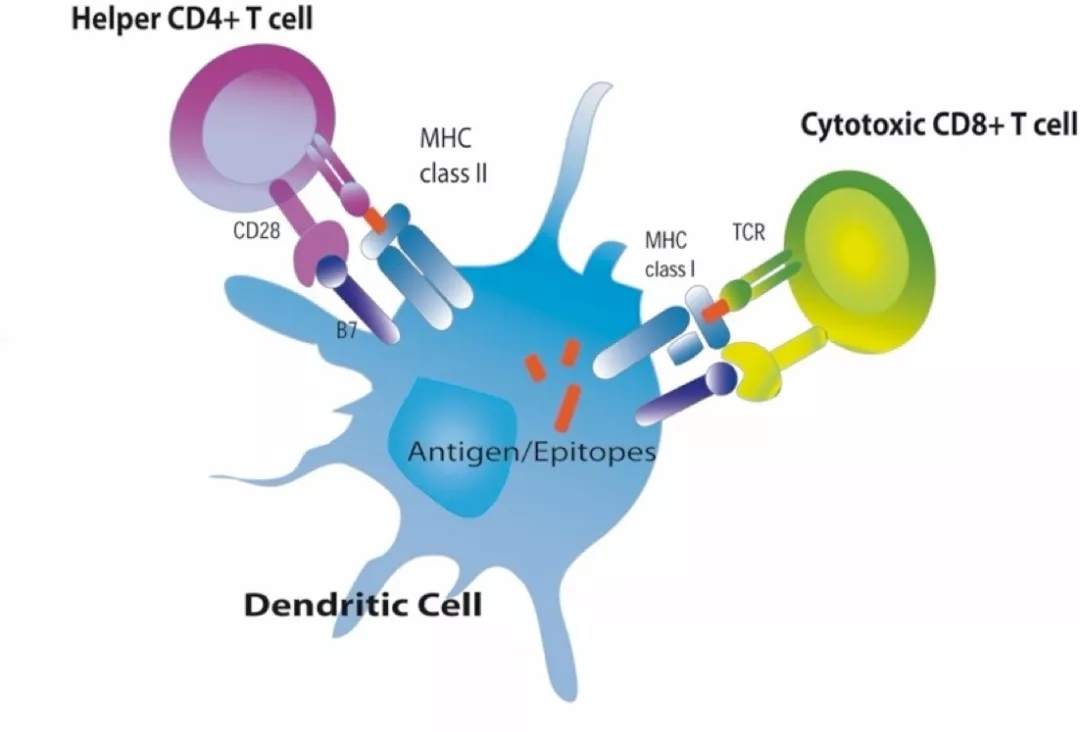
当然,识别抗原还少不了抗原提呈细胞(ADC)的参与
(图片来源:波士顿大学)
但单靠效应T细胞激活的免疫应答,往往不足以消灭肿瘤,不然免疫检查点抑制剂疗法平均的客观缓解率,就不会是30%[3]了。影响疗效的原因有很多,但归根结底都和免疫细胞有关,科研的焦点,就自然转移到了曾经的“配角”身上。
2014年,《科学》上首次发表了利用靶向特定突变的CD4+T细胞疗法,治疗晚期癌症的报告[4],证实了辅助性T细胞免疫应答的存在。此后在2015和2017年,两例采用肿瘤疫苗,激活辅助性T细胞抗癌的案例先后登上《自然》[5-6]。
然而此前也提到过,MHCII类新抗原在癌细胞表面表达水平一般很低,和使用疫苗时的抗原数量根本没得比,人体正常也不会有过继性细胞疗法那么多的辅助性T细胞。
那么在应对“正常”的癌细胞,进行免疫检查点抑制剂治疗时,辅助性T细胞识别MHCII类新抗原,激活的免疫效应,作用到底有多大呢?
别看效应T细胞把癌细胞围住了,但有可能只是围而不攻
(图片来源:NIH)
这就是本次研究的团队想要解开的谜题。首先,为了尽量排除已知抗原激活免疫应答的影响,研究团队特地选择了免疫原性很低,免疫检查点抑制剂治疗基本无效的一个恶性肉瘤细胞系,给这些癌细胞插上MHCI类和II类新抗原来展开实验。
由于已被确认的MHCII类限定分子新抗原很少,研究团队借助算法模拟预测的方式,才找到一种仅可以被辅助性T细胞识别的MHCII类新抗原,命名为mITGB1,对应的还有仅可以被效应T细胞识别的MHCI类新抗原(mLAMA4)。
把新抗原表达不同的肉瘤细胞,注射到小鼠体内时,单独表达mITGB1或者mLAMA4的癌细胞,并不能诱导抗癌免疫应答,肿瘤该怎么长怎么长;但两种新抗原同时表达时,肿瘤的生长速度却变慢了,明显是受到了免疫应答的杀伤!
使用PD-1抑制剂+CTLA-4单抗联合治疗时,肿瘤更是完全消失了。如果把mITGB1和mLAMA4,换成两种只能被效应T细胞识别的MHCI类新抗原,免疫治疗的疗效就基本消失了。这说明激活免疫重要的是抗原类型,而不是抗原量。
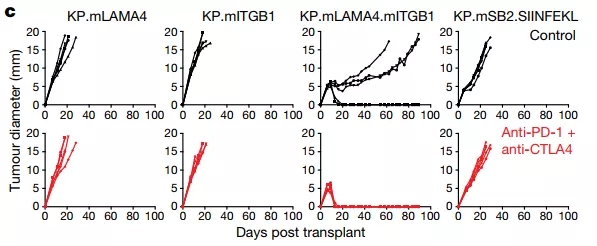
只有第三组:同时表达两种新抗原的肿瘤,能够被联合免疫治疗干掉,说明免疫应答的激活,两类新抗原缺一不可
只表达mITGB1或者mLAMA4的肿瘤,治疗后都不会消失,也就是说在研究团队营造的战场中,不管是效应T细胞还是辅助T细胞,识别抗原后,都不足以单独激活足够的抗肿瘤免疫。它们必须得同时找到相应的目标,然后协同作战才行。
T细胞亚群测定显示,浸润肿瘤的辅助性T细胞,亚型上74%是1型,和此前的研究相符。辅助性T细胞不仅可以使浸润肿瘤的效应T细胞数目增加,还能帮助它们增强杀伤力,数量质量两方面都有提高。
等等,这听着好像是辅助性T细胞的正常职责吧?一定要肿瘤表面有MHCII类新抗原,把辅助性T细胞从后方拉到前线,才能激活清除肿瘤的强力应答吗?
为了搞清这一点,研究团队在小鼠腹部的左右两侧分别植入了肿瘤,左侧的癌细胞同时表达两种新抗原,右侧的只表达mLAMA4,这就意味着辅助性T细胞只会在左侧肿瘤中识别抗原并发挥作用,右侧战场就是效应T细胞独挑大梁了。
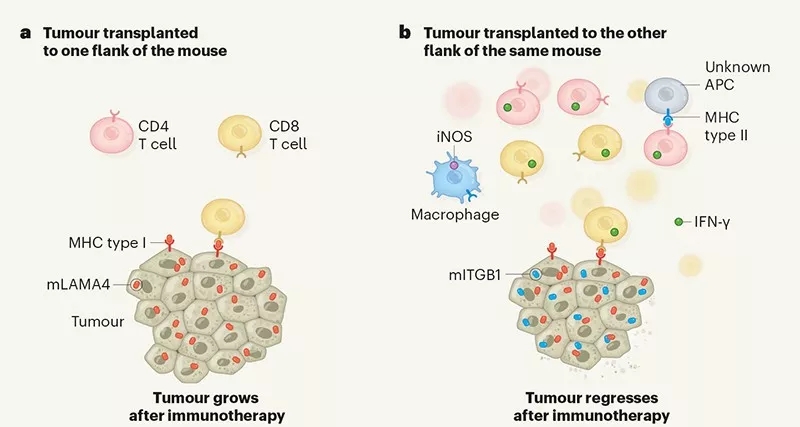
在同一只小鼠身上做两个肿瘤的试验,说服力就强了
事实证明,没有指挥官的部队打不了胜仗:小鼠左腹,同时表达两种新抗原的肿瘤,直接在注射免疫检查点抑制剂后被消灭了,而右腹只表达mLAMA4的肿瘤,接受同样的治疗,却仅仅是生长速度被拖慢了一点。差距真的有,不服不行。
实验还显示,辅助性T细胞还对维持小鼠的免疫记忆有着重要作用,不过它也不能当光杆司令。如果把这次实验中的辅助性T细胞单独注射到肿瘤部位,也就是采用与2014年《科学》上论文相似的过继性细胞疗法,一样控制不了肿瘤。
这一系列精彩的过程,倒不是只有辅助性T细胞和效应T细胞两位演员。实验中有一类巨噬细胞(iNOS+)的数量也暴增了83倍,研究团队认为,巨噬细胞可能是被辅助性T细胞分泌的干扰素-γ招募,增援了T细胞的作战。

作战地图上的“蓝方”是T细胞,面对“红方”癌细胞,“蓝方”还有紫色、黄色和绿色的不同免疫细胞当帮手
(图片来源:圣路易斯华盛顿大学)
从坐镇帅位到带头冲锋,这研究也算颠覆了过往对辅助性T细胞的认知。正如论文的通讯作者,圣路易斯华盛顿大学教授RobertSchreiber所说:“与效应T细胞相比,辅助性T细胞在免疫治疗上的研究和应用,落后得太多了。”
“免疫检查点抑制剂和肿瘤疫苗同时使用,是有不少先例的,但我们用激活辅助性T细胞的抗原当疫苗,效果要比此前的都好。我们希望它能把免疫检查点抑制剂疗法的客观缓解率,从20%(单独使用)提升到70%。”[7]
辅助性T细胞出手,让效应T细胞的杀伤力更上一层楼,如果真能转化到临床,绝对让人期待啊。
参考资料:
1.Alspach E, Lussier D M, Miceli A P, etal. MHC-II neoantigens shape tumour immunity and response to immunotherapy[J].Nature, 2019.
2.Gubin M M, Zhang X, Schuster H, et al.Checkpoint blockade cancer immunotherapy targets tumour-specific mutantantigens[J]. Nature, 2014, 515(7528): 577.
3.Haslam A, Prasad V. Estimation of thepercentage of US patients with cancer who are eligible for and respond tocheckpoint inhibitor immunotherapy drugs[J]. JAMA Network Open, 2019, 2(5):e192535-e192535.
4.Tran E, Turcotte S, Gros A, et al. Cancerimmunotherapy based on mutation-specific CD4+ T cells in a patient withepithelial cancer[J]. Science, 2014, 344(6184): 641-645.
5.Kreiter S, Vormehr M, Van de Roemer N, etal. Mutant MHC class II epitopes drive therapeutic immune responses tocancer[J]. Nature, 2015, 520(7549): 692.
6.Ott P A, Hu Z, Keskin D B, et al. Animmunogenic personal neoantigen vaccine for patients with melanoma[J]. Nature,2017, 547(7662): 217.
7.https://medicine.wustl.edu/news/clues-to-improve-cancer-immunotherapy-revealed/
头图来源:《科学》
(来源于:奇点糕 奇点网)


.png)